一、整体评价
本张试卷较上份卷子难度有所降低,重视基础,稳中向好(doge)
二、试卷总览
链接:https://pan.baidu.com/s/1L9wWyQ_0ctoWxC0DDtwWdw
提取码:n6fx 作者:考LiN https://www.bilibili.com/read/cv21275428 出处:bilibili
三、题目选讲
9
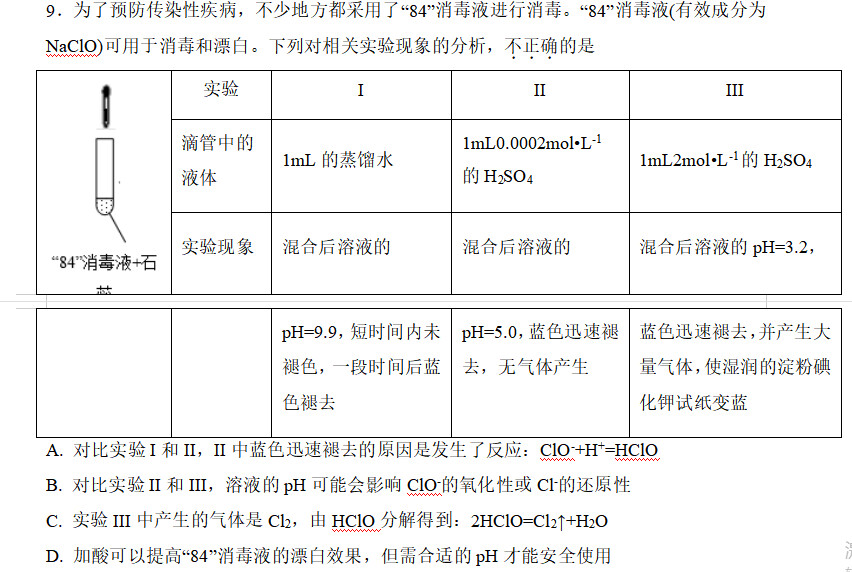
首先分析蓝色褪去原因:ClO-与氢离子结合生成强氧化性的次氯酸,次氯酸氧化了石蕊(有机物).A正确
产生气体使淀粉碘化钾试纸变蓝,只能是氯气。次氯酸如何产生氯气?和氯离子,在酸性环境归中。氯离子哪里来的?次氯酸氧化有机物后,自身得电子变成氯离子存在。
溶液的pH对氧化性有很大影响,次氯酸,如次氯酸氧化性强于次氯酸根(酸性条件不稳定,不稳定性决定了氧化性强)BD正确
C错误。次氯酸分解一般生成氧气和氯化氢,
所以本题选择C
11
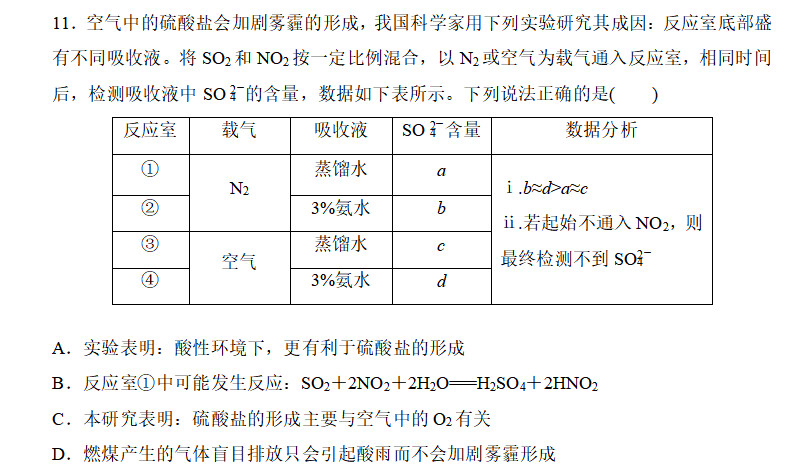
选择B 不难
说明:把二氧化硫和二氧化氮混合通入溶液,二氧化氮产生硝酸氧化二氧化硫,自身被还原,4价S变成硫酸根(+6)。蒸馏水和氨水起到调pH的作用。笔者认为碱性环境增大了二氧化硫、二氧化氮这样的酸性气体(姑且这样认为)的溶解度,因此二氧化硫溶解多,氧化的量自然就多。
12
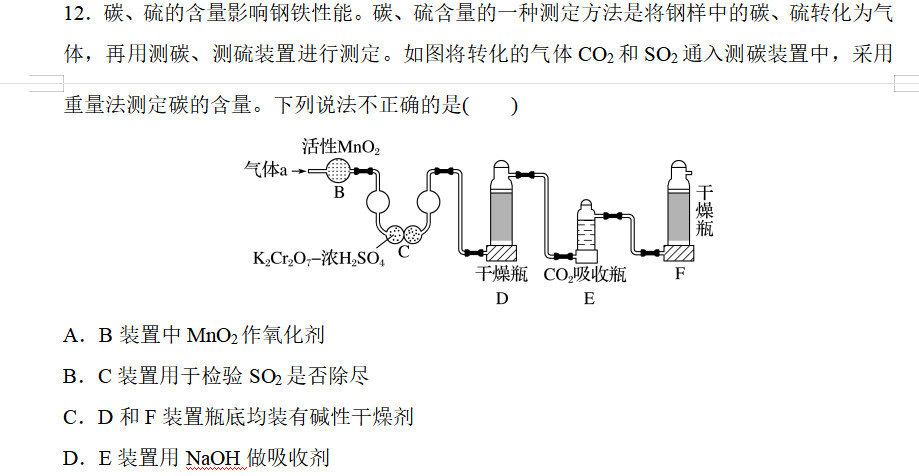
首先通过活性二氧化锰(应是湿)把二氧化硫氧化为硫酸,二氧化碳通过,接着C中的重铬酸钾应该是少量,起到指示的作用。如果有残余的二氧化硫可以与其反应,因此如果C中的橙色不变淡(无明显变化)则可以说明二氧化硫在B中已经完全除去。这时二氧化碳来到D中干燥,接着被E吸收。F可以防止外界二氧化碳和水进入E影响测定,可以选用碱石灰等干燥。
C选项:如果D中装有碱性干燥剂,那么也会吸收二氧化碳,影响E测定结果,不正确。
18-2

18-3
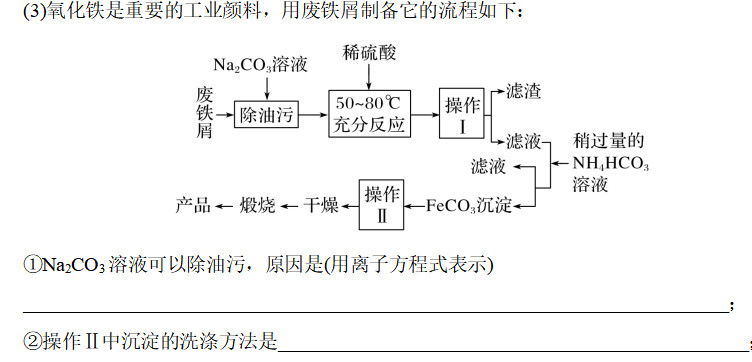
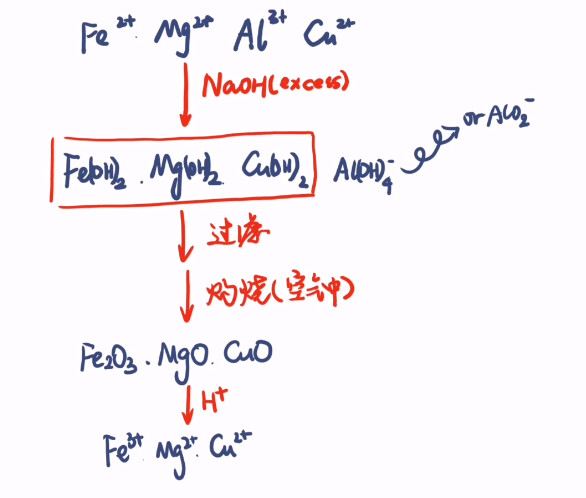
沉淀的洗涤方法:如图所示
向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次


联系:2020江苏


其实我认为,这道题除了水洗之外还应该增设一个醇洗的步骤,理由如下:
碳酸亚铁露置在潮湿空气中极易被氧化,故应该尽快移除水分,避免与空气接触,应该用酒精洗涤加快表面水分蒸发。
*相关例题:

盐酸酸化氯化钡:检验最后一次洗涤液
乙醇:作用如上
19
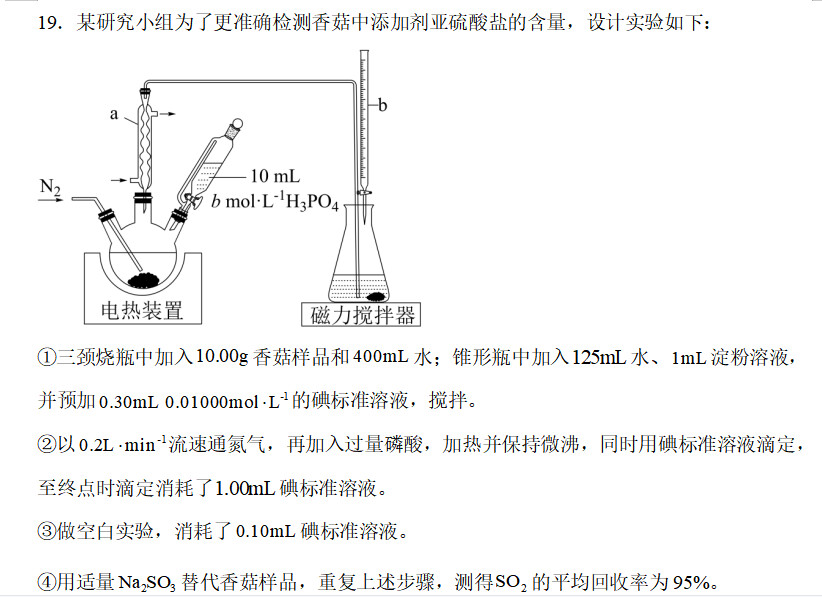

(3)形成二氧化硫原因:
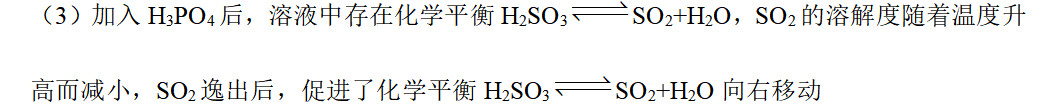
但是笔者认为,溶液存在诸多平衡,只叙述一个平衡是不合适的
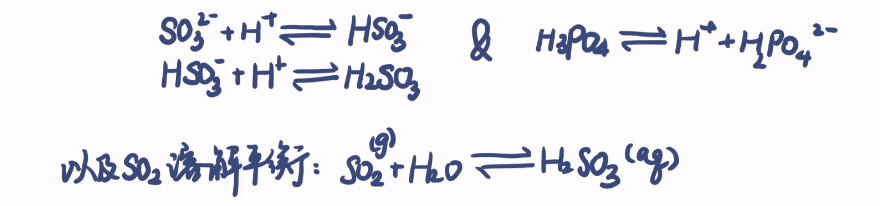
首先,亚硫酸氢根的K远小于H3PO4的Ka1,所以完全可以认为所有的亚硫酸根都转化为了亚硫酸氢根。那么问题的关键在于凭什么磷酸的酸性弱于亚硫酸,仍然可以把亚硫酸氢根转化为亚硫酸根。
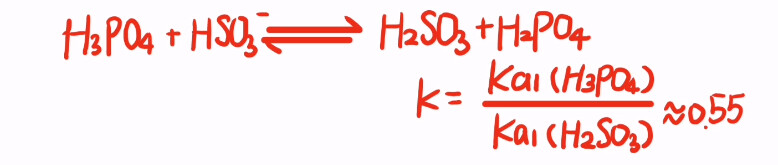
反应平衡常数不大不小,所以这是个典型的化学平衡。考虑到加入了6mol每升的浓磷酸,使得磷酸的浓度大大增加,促使平衡向正反应发生,溶液中亚硫酸浓度增加。然后再是标准答案给的二氧化硫与亚硫酸的平衡向着二氧化硫方向移动。
(5)滴定

注意要点:
1、什么叫空白实验?空白实验排除了非实验材料因素引起的滴定消耗,可消除或减少由试剂、蒸馏水或器皿带入的杂质所造成的系统误差。空白试验是在不加入试样的情况下,按与测定试样相同的步骤和条件进行的试验。
2、二氧化硫的回收率仅95%:可能是亚硫酸根在空气中可能被氧化为硫酸根,碘的耗量就会偏小,导致二氧化硫回收率比100%略低
(5)误差分析

通氮气经典作用:排出装置内的空气,防止其氧化4价硫。所以氮气后通入,测定结果偏低(一部分被氧气消耗掉,就没必要用更多的碘来氧化了)
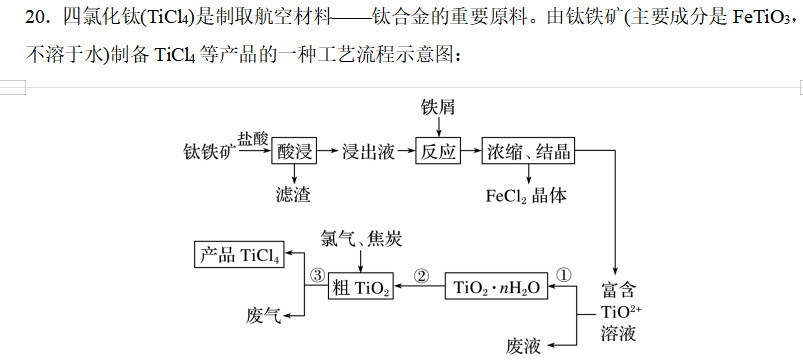

加入铁屑可以还原生成的三价铁。避免三价铁把钛离子氧化为TiO2+。
